7月9日�,醫(yī)療網(wǎng)絡(luò)體外診斷產(chǎn)業(yè)是醫(yī)療器械吸引器的重要子領(lǐng)域�����,也是投資者關(guān)注的重點(diǎn)投資領(lǐng)域之一��。根據(jù)檢測(cè)原理�,體外診斷可分為生化診斷��、免疫診斷和分子診斷�。分子診斷細(xì)分行業(yè)處于發(fā)展階段,臨床應(yīng)用逐漸擴(kuò)大����。它是最具創(chuàng)新性和增長(zhǎng)最快的體外診斷市場(chǎng)。
在分子診斷領(lǐng)域����,隨著國(guó)內(nèi)發(fā)展的發(fā)展����,許多創(chuàng)新產(chǎn)品得到了批準(zhǔn)���;液體活組織檢查和非侵入式癌癥早期篩查仍處于萌芽階段,國(guó)內(nèi)企業(yè)可以積極追求國(guó)外巨頭����;在基因測(cè)序領(lǐng)域,光照系列是最大的和第三的���,第四代測(cè)序技術(shù)尚不成熟��。
伴隨診斷(CDX)是一種與靶向藥物相關(guān)的體外診斷技術(shù)�。主要測(cè)量人體蛋白質(zhì)和突變基因的表達(dá)水平���,了解不同患者對(duì)特定藥物的治療反應(yīng)����,篩選最合適的用藥者�����,并進(jìn)行有針對(duì)性的個(gè)體化治療。
伴隨的診斷也可以很容易地理解為一個(gè)診斷是與目標(biāo)藥物發(fā)展���。1998年�,乳腺癌治療藥物曲妥珠單抗(trastuzumab)批準(zhǔn)了第一個(gè)同時(shí)進(jìn)行的HER2/neu診斷試驗(yàn)�����。預(yù)計(jì)到那時(shí)�����,中國(guó)的市場(chǎng)份額將達(dá)到6.5%��,伴隨中國(guó)的診斷市場(chǎng)預(yù)計(jì)將達(dá)到50億元左右����。
高通量測(cè)序技術(shù),又稱下一代測(cè)序技術(shù)(NGS)���,在檢測(cè)未知序列���、未知突變和高通量多位點(diǎn)檢測(cè)等方面具有優(yōu)勢(shì)�。與通常用于診斷領(lǐng)域的PCR相比��,它適用于乳腺癌易感基因(BRCA)等成千上萬個(gè)突變位點(diǎn)的目標(biāo)檢測(cè)��。NGS是伴隨診斷領(lǐng)域的一個(gè)研究和發(fā)展熱點(diǎn)��。自2016年以來�����,四種產(chǎn)品已獲準(zhǔn)在美國(guó)上市�。
中國(guó)在研究和發(fā)展NGS方面�,跟隨美國(guó)的步伐。2018年�,燃料石醫(yī)學(xué)、NOAH起源����、南京石河、艾德生物等NGS伴隨診斷產(chǎn)品相繼獲批�����。前三家公司的NGS產(chǎn)品只適用于非小細(xì)胞肺癌�����。它們的目標(biāo)是對(duì)egfr、alk和ros1的基因突變�,而艾德生物體被批準(zhǔn)為伴隨診斷產(chǎn)品“人類10基因突變聯(lián)合檢測(cè)”。該試劑盒(可逆的端到端測(cè)序)是第一個(gè)交叉癌分析����,納入Kras野生型分析,以應(yīng)對(duì)結(jié)直腸癌����。
NGS聯(lián)合檢測(cè)試劑盒是PCR產(chǎn)物的重要補(bǔ)充,主要用于具有更多突變位點(diǎn)的基因檢測(cè)和用于腫瘤檢測(cè)的大面板平臺(tái)����。未來幾個(gè)技術(shù)平臺(tái)將繼續(xù)與診斷共存,PCR技術(shù)仍將是現(xiàn)階段(3年)的主要伴隨診斷�。
基因測(cè)序
基因測(cè)序技術(shù)誕生于1975,為在遺傳水平上篩查疾病和診斷病因奠定了技術(shù)基礎(chǔ)��。21世紀(jì)初�����,在21世紀(jì)初,Roche公司的Roche公司���、Solexa和Hidseq技術(shù)的Roche公司����、Solexa和Hidseq技術(shù)在此之前�,人類基因組測(cè)序需要三年時(shí)間,而使用第二代測(cè)序技術(shù)只需一周時(shí)間��。
與第二代測(cè)序技術(shù)相比�����,第三代和第四代測(cè)序技術(shù)在讀取長(zhǎng)度和測(cè)序速度上具有很大優(yōu)勢(shì)���,但在通量和精度上存在不足。
目前�����,基因測(cè)序在臨床診斷和治療中有著廣泛的應(yīng)用����,尤其是在癌癥、產(chǎn)前診斷和遺傳病等領(lǐng)域。根據(jù)華達(dá)的招股說明書數(shù)據(jù)��,全球基因測(cè)序市場(chǎng)近年來發(fā)展迅速����,從2007年的7.94億美元發(fā)展到2015年的59億美元。預(yù)計(jì)未來幾年將繼續(xù)快速增長(zhǎng)�,2020年達(dá)到138億美元,復(fù)合年增長(zhǎng)率18.7%�。
世界上最大的測(cè)序器制造商是美國(guó)的照明公司。Illumina在2017年賺得27.52億美元����,占全球基因測(cè)序器市場(chǎng)的80%以上。Illumina在2018年以12億美元收購了太平洋生物科學(xué)公司��,將太平洋生物公司的長(zhǎng)讀和長(zhǎng)序列技術(shù)與自己的高通量����、短讀和長(zhǎng)序列平臺(tái)相結(jié)合,創(chuàng)造了主導(dǎo)地位���。
預(yù)計(jì)納米孔(Nanopore)測(cè)序技術(shù)將成為第四代測(cè)序技術(shù)���。
2018年��,Guardant和AstraZeneca達(dá)成合作協(xié)議�����,為AstraZeneca的Oshitinib開發(fā)Guardant 360 CDx測(cè)試��,并向FDA申請(qǐng)注冊(cè)�。該試驗(yàn)適用于對(duì)奧西汀有反應(yīng)的微創(chuàng)血液試驗(yàn)患者�。Guardant還使用GuardantOmni平臺(tái)開發(fā)用于腫瘤突變負(fù)荷的基于血漿的(TMB)評(píng)分CDX測(cè)試。本試驗(yàn)將用于預(yù)測(cè)阿斯利康腫瘤研發(fā)管道中患者對(duì)免疫治療和靶向治療的反應(yīng)�。FDA已授予瓜蘭特OMNI診斷儀突破性的醫(yī)療設(shè)備識(shí)別,用于檢測(cè)基于血漿的TMB評(píng)分����。 無創(chuàng)癌癥早篩
Exas的共同守護(hù)者代表了無創(chuàng)癌癥篩查的技術(shù)前沿。2014年����,美國(guó)食品和藥物管理局批準(zhǔn)Cologard作為第一種早期篩查結(jié)直腸癌的方法����。EXAS通過糞便DNA和血液生化標(biāo)志物篩選大腸癌。大量臨床試驗(yàn)證實(shí)�����,結(jié)腸鏡在一般高危人群中篩查結(jié)直腸癌的敏感性為92%,篩查結(jié)直腸癌癌前病變的敏感性為69%��,總體特異性為87%�。Cologard由美國(guó)癌癥協(xié)會(huì)和國(guó)家綜合癌癥網(wǎng)絡(luò)推薦。
2018年��,EXAS公司獲得了4.54億美元的利潤(rùn)�����,沒有盈利���,市值約為111.8億美元�����,增長(zhǎng)了154.9倍��,這是過去十年制藥股的最大增幅(超過110億美元)���。

 吸引器
吸引器 高頻電刀
高頻電刀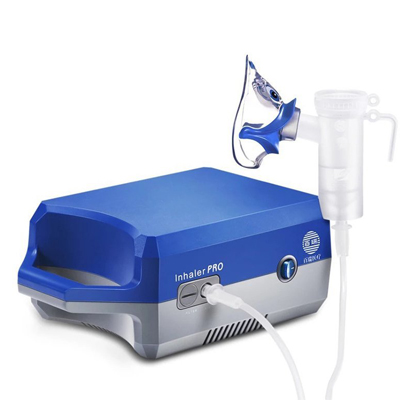 霧化器
霧化器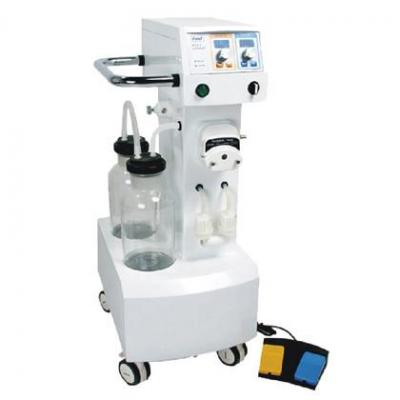 吸脂機(jī)
吸脂機(jī) 洗胃機(jī)
洗胃機(jī)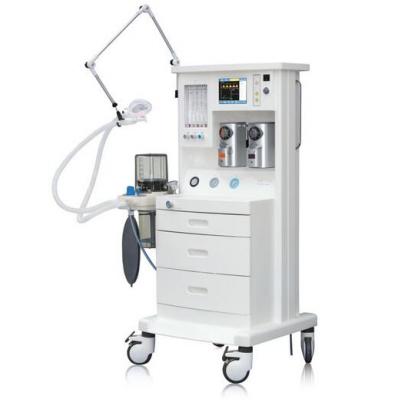 麻醉機(jī)
麻醉機(jī)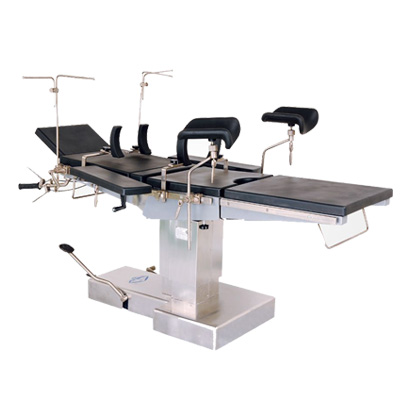 手術(shù)臺(tái)
手術(shù)臺(tái) 無影燈
無影燈
 400-006-1850
400-006-1850 滬公網(wǎng)安備 31011502008791號(hào)
滬公網(wǎng)安備 31011502008791號(hào)